Scholars Journal of Medical Case Reports
Titre abrégé : Sch J Med Case Rep
ISSN : 2347-9507 (Imprimé) | ISSN 2347-6559 (En ligne)
Site web du journal : https://saspublishers.com
Domaine : Chirurgie Générale
Volvulus Cæcal Aigu : Rapport de Cas et Revue de la Littérature
YASSINE Mohamed¹*, KALLOUT Ibrahim², MAZZOUR Oussama², JBILOU Aymane², AGGOURI Younes², AIT LAALIM Said²
¹ Département de Chirurgie Générale et d’Oncologie Digestive, Centre Hospitalier Universitaire Mohammed VI de Tanger, Maroc
² Faculté de Médecine et de Pharmacie de Tanger, Université Abdelmalek Essaadi, Tanger
DOI : https://doi.org/10.36347/sjmcr.2025.v13i06.00X
Reçu : 05.05.2025 | Accepté : 10.06.2025 | Publié : N/A
*Auteur correspondant : YASSINE Mohamed
Département de Chirurgie Générale et d’Oncologie Digestive, Centre Hospitalier Universitaire Mohammed VI de Tanger, Maroc
RÉSUMÉ
Rapport de cas
Le volvulus cæcal est le deuxième type de volvulus colique le plus fréquent, après le volvulus sigmoïde [1]. Il survient en raison d’une torsion ou d’une hyperflexion d’un cæcum élargi, mal fixé et hypermobile [2]. Cliniquement, il se présente sous la forme d’une occlusion intestinale aiguë, souvent accompagnée d’une strangulation. La tomodensitométrie abdominale (TDM / Scanner) fournit des informations diagnostiques cruciales [1]. La prise en charge initiale doit donner la priorité à une réanimation adéquate, avec des décisions thérapeutiques adaptées à des facteurs tels que l’âge du patient, ses antécédents médicaux, la viabilité du côlon et l’état clinique général [3]. Le traitement optimal implique une excision chirurgicale, la résection iléo-cæcale et l’hémicolectomie droite démontrant les meilleurs résultats [4]. Dans cet article, nous discutons d’un cas rare de volvulus survenant à l’âge de 64 ans, accompagné d’une revue de la littérature pour clarifier son diagnostic et sa prise en charge.
Mots-clés : Occlusion intestinale, volvulus, cæcum, hémicolectomie droite.
Copyright © 2025 L’auteur(s) : Ceci est un article en libre accès distribué selon les termes de la licence internationale Creative Commons Attribution 4.0 (CC BY-NC 4.0) qui permet une utilisation, une distribution et une reproduction sans restriction sur n’importe quel support, à condition que l’auteur original et la source soient crédités, pour une utilisation non commerciale.
INTRODUCTION
La première description du volvulus cæcal est attribuée à Rokitansky en 1837 [1]. Cette pathologie semblait rare car elle n’était responsable que de 1 % des obstructions intestinales [2]. Malgré de nombreuses publications, la symptomatologie et la prise en charge de cette affection restent controversées [2,3]. Nous rapportons ici l’observation de notre deuxième cas, traité aux urgences pour un volvulus cæcal, six ans après l’ouverture de notre département.
PRÉSENTATION DU CAS
Un homme de 64 ans originaire du Maroc, sans antécédents médicaux significatifs, a été admis aux urgences présentant des signes d’obstruction intestinale. Il présentait un syndrome occlusif caractérisé par une absence de gaz et de selles, accompagnée de vomissements. L’état général du patient est resté stable. Ces symptômes se sont développés progressivement au cours des cinq derniers jours.
Le patient était conscient et afébrile. Il présentait une tachycardie avec une fréquence cardiaque de 102 battements par minute, et une pression artérielle de 100/80 mmHg. L’oxymétrie de pouls affichait 96 % à l’air ambiant, et la fréquence respiratoire était de 25 cycles par minute. Des signes de déshydratation étaient manifestes, incluant un pli cutané et une muqueuse buccale sèche. L’examen abdominal a révélé une distension et une sensibilité à la palpation, avec un hypertympanisme. Les orifices herniaires étaient libres de toute hernie. Le toucher rectal a révélé une ampoule rectale vide.
Biologie : Globules blancs à 5000 éléments/mm3, Protéine C-réactive (CRP) à 210 mg/L, fonction rénale correcte (urée = 0,3 g/l, créatinine = 10 mg/l) et déséquilibre ionique avec hypokaliémie (potassium = 3 mmol/L).
Imagerie Médicale :
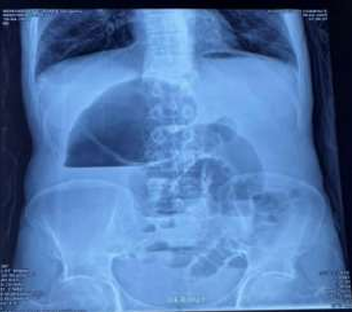
Radiographie de l’abdomen (ASP) : Position debout. Niveau hydro-aérique dans le cæcum gonflé. Anses iléales remplies de gaz latéralement au cæcum (fig 1).
Citation : YASSINE Mohamed, KALLOUT Ibrahim, MAZZOUR Oussama, JBILOU Aymane, AGGOURI Younes, AIT LAALIM Said. Volvulus Cæcal Aigu : Rapport de Cas et Revue de la Littérature. Sch J Med Case Rep, Juin 2025 ; 13(6) : N/A.
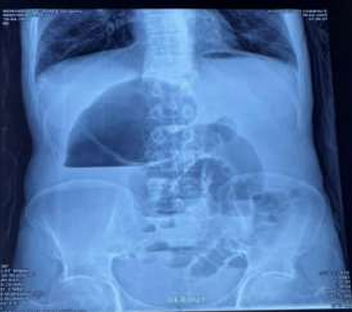
Figure 1 : Niveau hydro-aérique (NHA) volumineux reflétant la distension du cæcum.
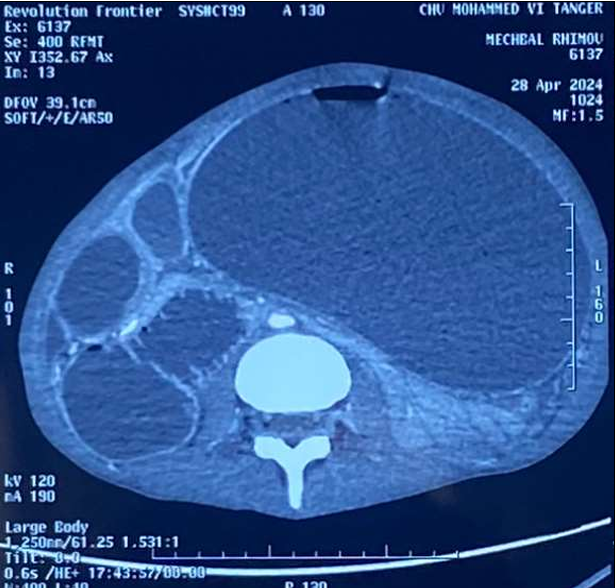
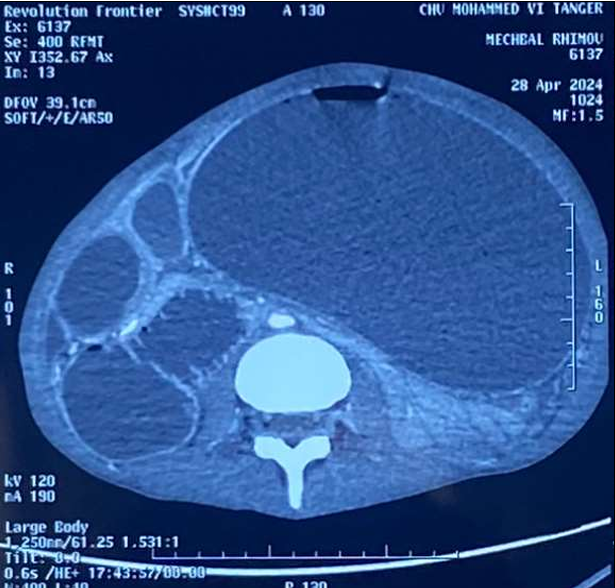
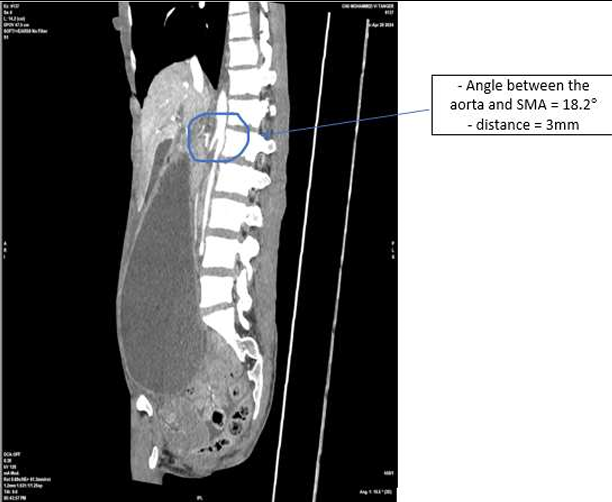
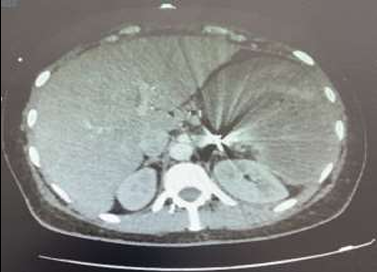
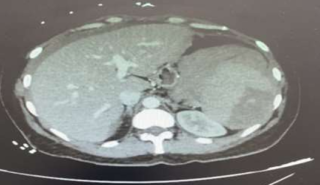
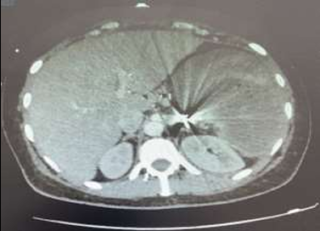
Le scanner abdominal injecté, sur les trois coupes de la tomodensitométrie avec produit de contraste durant la phase portale, montre une obstruction colique mécanique s’étendant jusqu’à 86 mm au niveau du cæcum, en amont d’une zone de transition formant une torsion en forme de tourbillon (Signe du tourbillon / Whirlpool sign) impliquant le côlon transverse et le pédicule vasculaire mésentérique, avec des signes de souffrance intestinale caractérisés par une pneumatose de la paroi intestinale (fig 2).
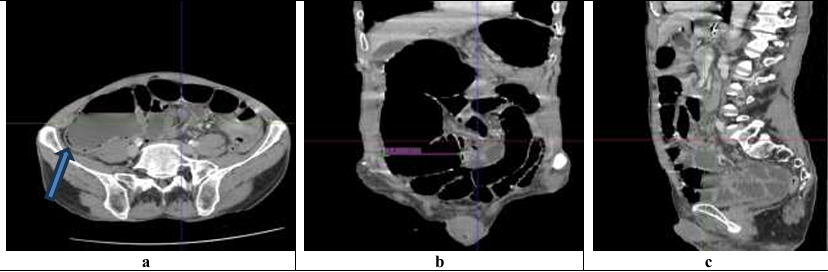
Figure 2 : Une obstruction colique mécanique est visible, s’étendant jusqu’à 86 mm au niveau du cæcum, en amont d’une zone de transition formant une torsion en forme de tourbillon (Signe du tourbillon / Whirlpool sign) impliquant le côlon transverse et le pédicule vasculaire mésentérique, avec des signes de souffrance intestinale caractérisés par une pneumatose de la paroi intestinale.
Après l’évaluation initiale, la décision a été prise de réaliser une intervention chirurgicale sur le patient. En per-opératoire, nous avons noté un volvulus iléo-cæco-colique, avec des signes de souffrance pariétale (fig 3, 4).
[FIGURE 3 – À INSÉRER ICI : PHOTO DE CHIRURGIE]
Figure 3 : Volvulus iléo-cæco-colique. On note la présence d’un appendice en haut et au milieu.
[FIGURE 4 – À INSÉRER ICI : PHOTO DE CHIRURGIE]
Figure 4 : Démonstration de trois tours (torsions) entre l’iléon, le cæcum et le côlon ascendant avec des signes de souffrance de la paroi intestinale.
Nous avons réalisé une hémicolectomie droite avec une anastomose iléo-transverse latéro-terminale (fig 5). Les suites postopératoires immédiates et à six mois ont été sans particularité. L’examen anatomopathologique n’a révélé aucun signe de malignité.
[FIGURE 5 – À INSÉRER ICI : PHOTO DE LA PIÈCE OPÉRATOIRE]
Figure 5 : Pièce chirurgicale d’hémicolectomie droite.
DISCUSSION
Le volvulus est une pathologie dans laquelle une anse intestinale et son mésentère se tordent autour d’un point fixe à la base de référence. Cela survient lorsqu’un segment long et mobile du côlon possède une attache mésentérique étroite et fixe, ce qui permet facilement une rotation axiale [5]. Une fois tordus, les gaz et les fluides s’accumulent dans l’anse obstruée, entraînant une distension, une ischémie, une gangrène et une perforation [6]. Le volvulus peut survenir au niveau du côlon sigmoïde, du cæcum, de l’angle splénique et du côlon transverse, par ordre décroissant de fréquence [7].
Le volvulus cæcal représente 10 à 40 % des volvulus coliques [1]. Il peut être divisé en deux sous-groupes : le volvulus iléo-colique axial, qui représente 90 % des cas, et la bascule cæcale, qui représente 10 % des cas [4]. Dans le volvulus iléo-colique classique, la torsion est généralement une rotation antihoraire de façon oblique, déplaçant également l’iléon [1,4,8]. Dans la bascule cæcale, le cæcum pivote dans un plan horizontal vers le haut et l’avant, avec l’obstruction située au point de pliage [1,4].
Un prérequis indispensable à la survenue d’un volvulus cæcal est une mobilité anormale du cæcum résultant d’une fusion embryonnaire incorrecte du mésentère du cæcum et du côlon ascendant avec le péritoine pariétal postérieur dans la gouttière droite [9]. Malgré cette prédisposition anatomique, la cause et les facteurs favorisants sont multifactoriels et incluent les adhérences ainsi que les manipulations chirurgicales récentes [1,4,8,9].
COURTY a divisé le volvulus du côlon droit en trois types : cæco-colique, iléo-cæco-colique et torsion axiale. Ce dernier type semble être similaire au premier [1].
L’intensité des signes cliniques et des symptômes varie en fonction de la portion intestinale impliquée ainsi que du degré et de la durée de la torsion [8]. Douleur abdominale généralisée (90 %), distension abdominale (80 %) la constipation (60 %) et les vomissements (28 %) sont des symptômes courants [4].
Voici la traduction intégrale et fidèle de la quatrième page de votre article (page 4 du journal). Cette partie traite du diagnostic différentiel, des options chirurgicales détaillées et de la conclusion.
YASSINE Mohamed et al, Sch J Med Case Rep, Juin 2025 ; 13(6) : N/A
…la constipation (60 %) et les vomissements (28 %) sont des symptômes courants [4].
Le diagnostic repose rarement uniquement sur les signes cliniques, et la radiographie abdominale (ASP) joue un rôle essentiel. Le côlon dilaté présente un niveau hydro-aérique unique qui peut se trouver n’importe où dans l’abdomen, selon sa position initiale, le degré de distension gazeuse, le site, ainsi que le degré et la durée de la torsion. Il est typique d’observer des anses de l’intestin grêle distal sur le côté droit du côlon dilaté, tandis que le côlon distal contient peu de gaz.
D’autres signes radiologiques incluent le signe du grain de café et le signe du tourbillon (whirl sign) au scanner. Le diagnostic radiologique du volvulus cæcal peut être posé avec certitude dans 90 % des cas. Le diagnostic différentiel inclut la dilatation gastrique, le volvulus du sigmoïde, le volvulus de l’intestin grêle et l’obstruction colique avec une valve iléo-cæcale compétente [3,4].
Bien qu’il y ait eu des cas de décompression non opératoire réussie par colonoscopie, cette méthode n’est pas plébiscitée en raison d’un taux d’échec élevé [7,10,11]. Une chirurgie d’urgence est nécessaire pour la plupart des patients présentant un volvulus cæcal.
Lors de la laparotomie, la détermination de la viabilité de l’intestin est la première étape de la prise en charge. La suite du traitement dépend de l’état de l’intestin (viable ou gangrené). Un intestin non viable nécessite une excision immédiate de l’anse impliquée, ce qui peut être réalisé par une hémicolectomie droite. La détorsion simple dans ces circonstances est déconseillée, car il a été démontré qu’elle peut entraîner un choc septique irréversible [3].
La décision entre une anastomose primaire ou une iléostomie doit être basée sur l’état du patient et l’état de l’intestin au moment de la chirurgie [11,12]. La majorité des équipes préfèrent l’anastomose primaire d’un iléon terminal sain, bien que dilaté et non préparé, sur un côlon transverse viable et non dilaté [12].
Les procédures non réséctionnelles les plus couramment utilisées sont la cécopexie et la cécostomie. La cécopexie, en ancrant le côlon droit au péritoine pariétal, prévient la récidive du volvulus cæcal en éliminant l’hypermobilité préexistante [2]. La cécostomie a également été utilisée avec des résultats variables [13]. Elle implique l’insertion d’un tube de cécostomie par une petite incision dans la paroi cæcale, amenant le cæcum à la paroi abdominale antérieure et faisant sortir le tube par une petite incision cutanée. Elle présente l’avantage non seulement de fixer l’intestin, mais aussi de décompresser le segment distendu.
La colonoscopie peut être réalisée et montrer le volvulus ainsi qu’une ischémie colique pariétale plus ou moins profonde [14,15]. La détorsion endoscopique est réalisable en l’absence d’ischémie sévère, mais comporte un risque significatif de perforation [14,15].
Le traitement vise trois objectifs : lever l’obstacle par détorsion si possible, traiter les complications progressives et prévenir la récidive [16]. Cela reste controversé. L’hémicolectomie droite avec anastomose primaire est recommandée par plusieurs équipes, même en l’absence de nécrose colique, car elle élimine le risque de récidive. La cécostomie est efficace pour prévenir les rechutes mais présente un risque élevé d’infection de la paroi et de fistule digestive nécessitant une intervention de fermeture.
Les complications infectieuses sont moins fréquentes avec les cécopexies, mais les récidives y sont plus nombreuses. L’approche coelioscopique première [17] est rarement utilisée en urgence car elle provoque une distension du cæcum et des difficultés d’exposition. Elle pourrait être réalisée après détorsion et exsufflation endoscopique.
CONCLUSION
Le volvulus du cæcum est la deuxième cause de volvulus colique, après celle du côlon sigmoïde. Deux mécanismes sont décrits : la torsion (90 %) et la bascule (10 %). Le tableau clinique est celui d’une occlusion intestinale aiguë. La radiographie abdominale (ASP) permet le diagnostic dans plus de la moitié des cas en montrant un niveau hydro-aérique de l’intestin grêle et une distension cæcale avec absence d’air dans le côlon. Le scanner abdominal permet un diagnostic rapide en montrant l’image typique du signe du tourbillon et une distension cæcale majeure.
Le traitement doit être chirurgical : les réductions sous colonoscopie et les lavements hydrosolubles sont inefficaces. La chirurgie d’exérèse (résection iléo-cæcale et hémicolectomie droite) donne les meilleurs résultats immédiats et à long terme. La cécopexie doit être discutée en l’absence de nécrose et chez les patients âgés ou présentant de graves comorbidités. La cécostomie semble inadaptée au traitement de cette pathologie.
Déclaration de conflit d’intérêts : Aucun déclaré
Financement : Aucun
RÉFÉRENCES
-
Theuer C, Cheadle WG. Volvulus of the colon. Am Surg 1991; 57:257-262.
-
Wolfer JA, Beaton LE, Anson BJ. Volvulus of the cecum. anatomical factors in its etiology. Surg Gyn Obst 1942;882-94.
-
Madiba TE, et al. The Management of Cecal Volvulus. DOI: 10.1007/s10350-004-6158-4.
-
Abita T, Lachachi F, et al. Les volvulus du cæcum. Service Chirurgie Viscérale et Transplantation, CHU Dupuytren – Limoges.
-
Consorti ET, Liu TH (2005). Diagnosis and treatment of caecal volvulus. Postgraduate medical journal, 81(962), 772-776.
-
Avots-Avotins KV, et al. (1982). Volvulus colique chez le patient gériatrique. Surg Clin North Am, 62:249–60.
-
Ballantyne GH, et al. (1985). Volvulus du côlon : Incidence et mortalité. Ann Surg, 202:83–92.
-
Haskin PH, et al. (1981). Volvulus du cæcum et du côlon droit. JAMA, 245: 2433–5.
-
Shoop SA, et al. (1993). Cécopexie laparoscopique pour volvulus cæcal. Surg Endosc, 7:450–4.
-
Anderson MJ Sr, et al. (1978). Le colonoscope dans le volvulus cæcal : rapport de trois cas. Dis Colon Rectum, 21:71–4.
-
Anderson JR, et al. (1986). Volvulus aigu du côlon droit : Analyse de 69 patients. World J Surg, 10: 336 – 42.
-
Gupta S, et al. (1993). Volvulus cæcal aigu : rapport de 22 cas et revue de la littérature. Ital J Gastroenterol, 25:380 – 4.
-
Benacci JC, et al. (1995). Cécostomie : indications thérapeutiques et résultats. Dis Colon Rectum, 38:530–4.
-
Friedman JD, et al. (1989). Expérience avec le volvulus colique. Dis Colon Rectum, 32(1): 409.
-
Neil DA, et al. (1987). Volvulus cæcal : dix ans d’expérience dans un hôpital universitaire australien. Ann R Coll Surg Engl, 69(2): 283-285.
-
Katoh T, et al. (2009). Volvulus cæcal : Rapport d’un cas et revue de la littérature japonaise. World J Gastroenterol, 15(20): 2547-2549.
-
Shoop SA, et al. (1993). Cécopexie laparoscopique pour volvulus cæcal : rapport de cas et revue de la littérature. Surg Endosc, 7(5): 450-454.
© 2025 Scholars Journal of Medical Case Reports | Publié par SAS Publishers, India |